细菌秒变“肿瘤炸弹”!中科院黑科技登顶《CELL》
癌症免疫治疗通过激活患者自身的免疫系统来对抗肿瘤,已成为当下备受瞩目的抗癌新策略。然而,对于实体瘤的治疗,复杂的肿瘤微环境常常限制了免疫疗法的疗效。与此同时,细菌免疫治疗凭借其独特的肿瘤靶向能力和免疫调节潜力,逐渐崭露头角,成为癌症治疗领域的新星。其实,将细菌应用于癌症治疗的研究早在19世纪就已开始。但由于当时的技术限制,细菌疗法的安全性、可控性和疗效难以得到保障。随着放疗和化疗等更为直接的肿瘤杀伤手段的出现和广泛应用,细菌疗法的研究逐渐陷入停滞。
如今,细菌疗法面临一个看似矛盾的双重挑战:如何让细菌在躲避先天免疫系统攻击的同时,仅在肿瘤内部激发抗肿瘤免疫反应?这一难题一直是细菌疗法迈向临床应用的关键瓶颈。
3月4日,中国科学院深圳先进技术研究院刘陈立团队联合中国科学院上海营养与健康研究所肖意传团队,在国际顶尖学术期刊《CELL》上发表了一项突破性研究成果。他们揭示了细菌疗法背后的机制:通过利用肿瘤内免疫细胞白介素-10受体(IL-10R)高表达,而正常组织内免疫细胞低表达的特性,细菌能够巧妙地实现“靶向实体肿瘤、躲避先天免疫系统、杀伤癌细胞”的三重目标。这一发现不仅阐明了细菌免疫治疗的核心机制,更为新一代合成细菌疗法的设计提供了重要的理论指导,有望为癌症治疗带来新的突破。

近年来,合成生物学的蓬勃发展为肿瘤免疫治疗注入了新的活力,催生了一系列新型抗肿瘤细菌,为攻克癌症开辟了全新的研究路径。在最新的研究中,科学家们将定量合成生物学的前沿理念引入细菌治疗肿瘤的研究,通过设计具有精准靶向和高效抗肿瘤能力的合成细菌,深入剖析了细菌与肿瘤相互作用的核心机制。
研究团队以沙门氏菌为基础,成功构建了一种合成菌株。这种菌株能够在肿瘤组织中高效存活并迅速增殖,而在正常组织中则会被快速清除。其基因线路设计精妙,包含两大关键模块:一是缺氧响应系统,能在正常组织中触发细菌的自毁机制;二是李斯特菌溶血素O基因,帮助细菌穿透肿瘤的致密基质。实验结果显示,这种合成细菌在结肠癌、黑色素瘤、膀胱癌等多种肿瘤动物模型中展现了显著的治疗效果。
在进一步的研究中,团队对多种关键细胞因子进行了筛选,发现白介素-10(IL-10)在细菌治疗肿瘤的过程中扮演着至关重要的角色。通过定量分析,科学家们揭示了IL-10R在肿瘤中的CD8+ T细胞、巨噬细胞和中性粒细胞等多种免疫细胞上呈现高表达。这种高表达特性使得肿瘤内的免疫细胞能够在细菌介导下发挥其抗肿瘤作用。相比之下,正常组织中免疫细胞的IL-10R水平较低,细菌与这些免疫细胞的相互作用也与肿瘤中的截然不同,且细菌会被中性粒细胞迅速清除。
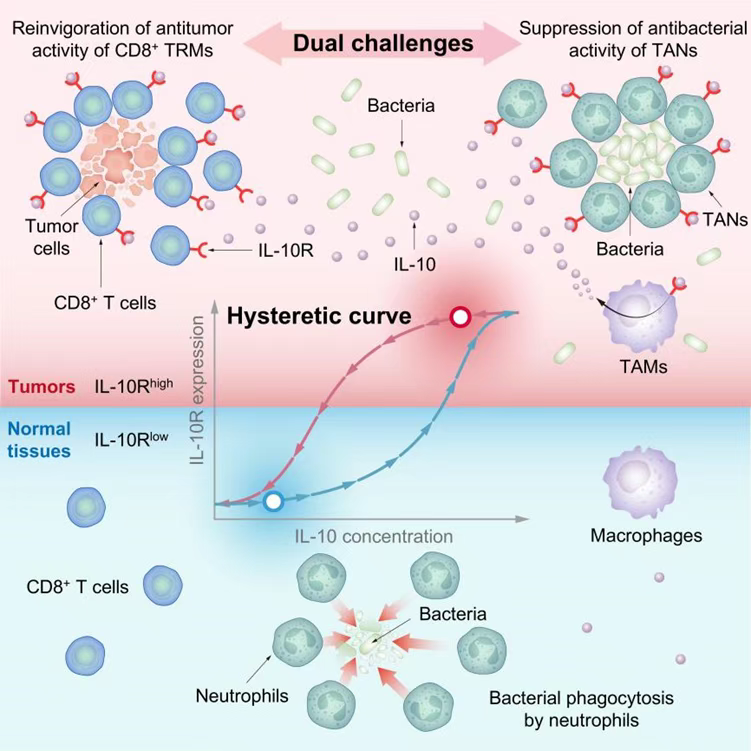
▲IL-10R迟滞效应导致了肿瘤微环境内的免疫细胞IL-10R高表达特性,细菌利用这一特性,同时实现了其避免被中性粒细胞快速清除,并激活肿瘤内组织驻留记忆CD8+ T细胞高效杀伤癌细胞。(图片来自《CELL》)
在探索细菌治疗肿瘤的过程中,研究团队意外发现了一个关键机制:细菌并非像传统认知那样通过趋化作用靶向肿瘤,而是利用其在肿瘤组织和正常组织中的差异化生长特性,实现了对肿瘤的“靶向”效果。这种差异化的生长机制不仅让细菌能够精准定位肿瘤,还揭示了它们在靶向实体瘤时如何做到“自保”(即逃避免疫系统的攻击)并有效杀伤肿瘤细胞。
这一发现为细菌治疗肿瘤领域带来了重大突破。它不仅清晰地解释了细菌如何在激活抗肿瘤免疫反应的同时,巧妙地逃避宿主的抗菌免疫反应,还解答了长期以来困扰该领域的关键科学问题——“为什么细菌能够做到激活抗肿瘤免疫,却又不引发抗菌免疫?”这一成果为未来细菌治疗肿瘤的研究和应用提供了重要的理论基础,也为开发新一代细菌疗法带来了新的希望。
