异种移植再登Nature:世界首例!我国学者将基因编辑的猪肝脏移植到人体内
在异种移植领域,中国科学家走在了世界前列
2025 年 3 月 27 日,空军军医大学西京医院窦科峰院士、王琳教授、董海龙教授、陶开山教授团队在国际顶尖学术期刊 Nature 上发表了题为:Gene-modified pig-to-human liver xenotransplantation 的研究论文。
01 异种移植的基础与临床研究取得里程碑式突破

最近几年,异种移植的基础与临床研究取得里程碑式突破。2021 年 10 月,纽约大学朗格尼医学中心首次将基因编辑的猪肾脏移植给了一位脑死亡女性。2022 年 1 月,马里兰大学医学院进行了世界首例活人移植基因编辑猪心脏的手术,患者在移植后存活了约 2 个月时间。这些突破在全世界范围内引发了广泛关注,让我们燃起了使用基因编辑猪作为供体进行异种移植来缓解人类器官移植短缺的希望。
该研究介绍了世界首例将基因编辑改造的猪肝脏移植到一名被诊断为脑死亡的人类受体的案例,该器官在脑死亡患者体内成功存活并正常工作 10 天。研究团队监测了 10 天内猪肝脏的功能、血流以及免疫和炎症反应。结果显示,猪肝脏在人体内正常运行并产生了胆汁和猪血清白蛋白,维持了稳定的血流,且没有出现排异迹象。这些结果表明,基因改造的猪肝脏能够在人体内存活并发挥功能,有望成为等待人类供体的肝衰竭患者的过渡疗法。
02 器官荒的救星:为什么选择猪?

全球每年有数百万患者因等不到器官移植而死亡。猪因其器官大小、生理功能与人类高度相似,被视为“天然器官库”。但直接移植会引发致命的免疫排斥反应——猪细胞表面的α-半乳糖抗原会让人体免疫系统发起超强攻击。
为此,中国科研团队对供体猪(巴马小型猪)进行了六基因改造:删除猪的三大“危险分子”基因:GTKO、CMAH 和 B4GALNT2,这三个猪基因会表达引起超急性排斥和急性体液性排斥的猪抗原;加入了三重“保护盾”基因:人类补体调节蛋白基因 hCD46、hCD55,人类凝血调节蛋白基因 hTBM,前两个人类基因能够抑制免疫攻击,第三个人类基因能够防止凝血紊乱。
03 一场精密的外科实验
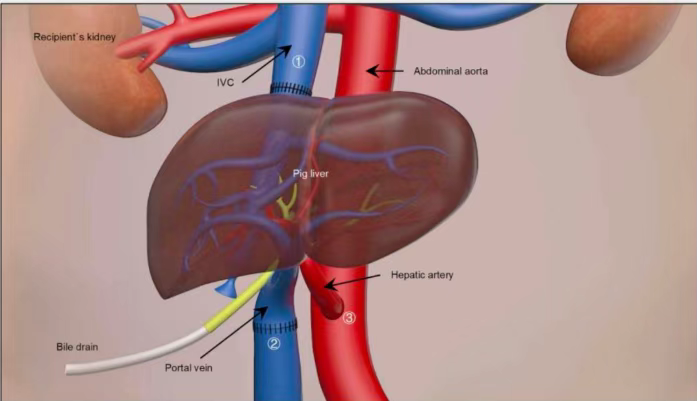
研究团队选择了一名被诊断为脑死亡但生命体征稳定的患者作为受体,在医院伦理委员会严格的监督下,研究团队采用异位辅助肝移植方案,将上述基因改造的猪肝脏移植到该脑死亡患者体内,而不切除患者原有肝脏(该手术于 2024 年 3 月 10 日进行)。移植手术后 10 天监测显示:
功能性指标:移植后 2 小时即产生金黄色胆汁,10 天内累计分泌 66.5 毫升;猪血清白蛋白持续升高; 血液动力学:肝动脉血流速度稳定在 41.45-60.63 cm/s; 无严重排斥:组织学检查显示肝脏再生良好,未发现典型排斥反应。
充免疫系统的“攻防战”
为控制排异反应,研究团队制定了多靶点免疫抑制方案:
术前:抗胸腺细胞球蛋白(清除T细胞)+ 补体抑制剂(防超急性排斥);
术后:他克莫司+霉酚酸酯(经典抗排异药)+ 利妥昔单抗(抑制B细胞活化)。
结果令人振奋:T 细胞活性被有效抑制,B 细胞虽在第 3 天短暂激活,但被及时控制。炎症因子(例如 IL-6、TNF-α)水平始终处于低位,补体沉积极少。
04 未来挑战与希望
虽然该研究仅持续 10 天,但已传递出关键信息:
安全性可控:未检测到猪内源性逆转录病毒(PERV)和猪巨细胞病毒(PCMV)传播;凝血难题突破:血小板和凝血时间波动后恢复正常,hTBM 基因显效。
窦科峰院士表示,这是医学界第一次将基因改造猪肝植入人体内,在目前观察的96小时内,移植的基因改造猪肝脏,在人体内能够发挥生理功能,正常分泌胆汁,说明有可能替代人类肝脏。该项研究的顺利开展,是异种器官移植领域的重大突破,也是异种肝移植向临床迈进的关键一步,为下一步的临床应用提供了理论依据和数据支撑。
从猪心脏、猪肾脏再到猪肝脏,异种移植正以惊人速度推进。或许不久的将来,“定制化猪器官”将彻底改写器官移植规则。这场生命科学的革命性突破,我们正在一同经历与见证!
素材来源官方媒体/网络新闻
